Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Đại cương về kim loại chuyển tiếp dãy thứ nhất SVIP
I. ĐƠN CHẤT KIM LOẠI CHUYỂN TIẾP DÃY THỨ NHẤT
1. Đặc điểm cấu tạo nguyên tử
Kim loại chuyển tiếp dãy thứ nhất gồm các nguyên tố từ Sc (Z = 21) đến Cu (Z = 29).
Câu hỏi:
@202874618271@
- Đặc điểm cấu hình electron nguyên tử:
+ Lớp vỏ bên trong của khí hiếm Ar.
+ Số electron trên phân lớp 3d tăng dần từ 1 đến 10.
+ Trên phân lớp 4s, số electron bằng 2 (trừ Cr và Cu bằng 1).
- Nguyên tử của kim loại chuyển tiếp có nhiều electron hóa trị nên tạo được nhiều hợp chất với số oxi hóa khác nhau.
2. Tính chất vật lí và ứng dụng của kim loại chuyển tiếp
Kim loại chuyển tiếp thường có nhiệt độ nóng chảy cao, độ cứng lớn, khối lượng riêng lớn, dẫn điện và dẫn nhiệt tốt nên được ứng dụng trong sản xuất thiết bị chịu nhiệt, công cụ cắt gọt, dây dẫn và thiết bị truyền nhiệt.
Đầu nối chịu nhiệt làm từ hợp kim của sắt |
Mũi khoan làm từ hợp kim của chromium |
Dây điện làm từ kim loại đồng |
Gang làm từ hợp kim của sắt |
II. HỢP CHẤT CỦA KIM LOẠI CHUYỂN TIẾP DÃY THỨ NHẤT
1. Số oxi hóa của nguyên tử kim loại chuyển tiếp dãy thứ nhất trong hợp chất
Các nguyên tố chuyển tiếp dãy thứ nhất có nhiều electron hóa trị (phân lớp 3d và 4s) nên khả năng tạo ra các hợp chất với nhiều trạng thái oxi hóa khác nhau.
Câu hỏi:
@202874615995@
Một số trạng thái oxi hóa thường gặp của kim loại chuyển tiếp dãy thứ nhất:
Nguyên tử | Cr | Mn | Fe | Cu |
Số oxi hóa | +3 +6 | +2 +4 +7 | +2 +3 | +2 |
Khi tham gia phản ứng, kim loại chuyển tiếp dãy thứ nhất thường nhường electron 4s trước rồi đến 3d để tạo các cation tương ứng.
Ví dụ 1:
Fe | → | Fe2+ | + | 2e |
[Ar]3d64s2 |
| [Ar]3d6 |
|
2. Màu sắc của các ion kim loại chuyển tiếp dãy thứ nhất
Các ion kim loại chuyển tiếp dãy thứ nhất có màu sắc phong phú.
Ví dụ 2:
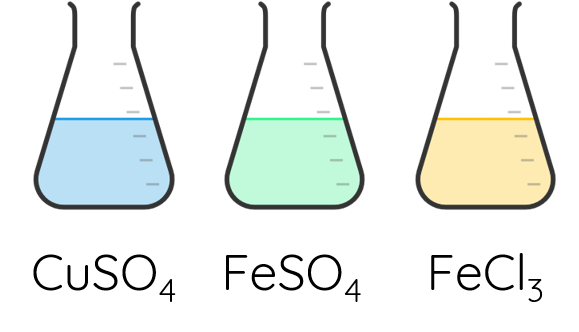
3. Chuẩn độ iron(II) sulfate bằng thuốc tím
Phản ứng chuẩn độ iron(II) sulfate bằng thuốc tím:
\(10FeSO_4+2KMnO_4+8H_2SO_4\rightarrow5Fe_2\left(SO_4\right)_3+2MnSO_4+K_2SO_4+8H_2O\)
⚡THÍ NGHIỆM (Xác định hàm lượng muối Fe(II) sulfate bằng dung dịch thuốc tím)
- Bước 1: Dùng pipette lấy 5,0 mL dung dịch FeSO4 cho vào bình tam giác. Dùng ống đong thêm vào khoảng 5 mL H2SO4 10%.

- Bước 2: Cho KMnO4 vào burette và điều chỉnh thể tích về mức 0.
- Bước 3: Mở khóa burette, nhỏ từng giọt KMnO4 vào bình tam giác, đồng thời lắc đều sau mỗi lần nhỏ. (Ban đầu dung dịch chuyển hồng rồi mất màu. Tiếp tục nhỏ đến khi màu hồng ổn định trong 20 giây thì kết thúc chuẩn độ).
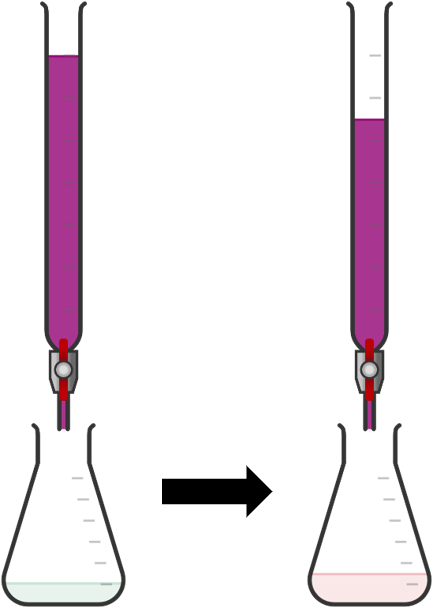
- Bước 4: Ghi lại thể tích dung dịch KMnO4 đã dùng. Tiến hành chuẩn độ 3 lần, lấy giá trị trung bình và tính toán.
Câu hỏi:
@205200424499@
4. Nhận biết một số ion kim loại chuyển tiếp
Các ion kim loại chuyển tiếp có thể được nhận biết nhờ màu sắc đặc trưng, sự tạo kết tủa ít tan hoặc phản ứng tạo phức chất.
⚡ THÍ NGHIỆM (Kiểm tra sự có mặt của từng ion riêng biệt: Cu2+ và Fe3+)
- Ống nghiệm 1: Thêm 2 - 3 giọt NaOH 1 M vào ống nghiệm chứa 2 mL dung dịch FeCl3 1 M.

- Ống nghiệm 2: Thêm 2 - 3 giọt NaOH 1 M vào ống nghiệm chứa 2 mL dung dịch CuSO4 1 M.

Câu hỏi:
@205395174536@
Bạn có thể đăng câu hỏi về bài học này ở đây




