Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Hợp chất carbonyl SVIP
I. KHÁI NIỆM, DANH PHÁP
1. Khái niệm
Hợp chất carbonyl là các hợp chất hữu cơ trong phân tử có chứa nhóm chức carbonyl (C=O).
- Aldehyde là hợp chất hữu cơ có nhóm –CHO liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc –CHO) hoặc nguyên tử hydrogen.
- Ketone là hợp chất hữu cơ có nhóm C=O liên kết với hai gốc hydrocarbon.
Ví dụ 1: Citronellal (aldehyde) có trong tinh dầu chanh.

Ví dụ 2: Menthone (ketone) có trong tinh dầu bạc hà.

Câu hỏi:
@201219670169@
2. Danh pháp
a. Danh pháp thay thế
- Aldehyde đơn chức: Tên hydrocarbon (bỏ e ở cuối) + “al”
- Ketone đơn chức: Tên hydrocarbon (bỏ e ở cuối) – vị trí nhóm C = O – “one”
Ví dụ 3: Aldehyde CH3CH=O có tên gọi là ethanal.
Ví dụ 4: Ketone CH3-CO-CH3 có tên gọi là propanone (acetone).
⚠ Chú ý:
- Chọn mạch carbon dài nhất chứa nhóm C=O.
- Mạch carbon đánh số từ nhóm -CHO hoặc từ phía gần nhóm C=O hơn.
- Nếu ketone chỉ có một vị trí C=O duy nhất thì không cần ghi số vị trí.
- Nếu mạch carbon có nhánh thì thêm vị trí, tên nhánh ở phía trước.
Câu hỏi:
@205396488906@@205396566280@
b. Tên gọi thông thường
Công thức | Tên thông thường |
|---|---|
HCHO | Aldehyde formic (formaldehyde) |
CH3CHO | Aldehyde acetic (acetaldehyde) |
C6H5CHO | Aldehyde benzoic (benzaldehyde) |
CH3COCH3 | Acetone |
II. ĐẶC ĐIỂM CẤU TẠO
Liên kết đôi C=O phân cực về phía nguyên tử oxygen:

Ví dụ 5: Mô hình phân tử của aldehyde và ketone.
Methanal |
Acetone |
III. TÍNH CHẤT VẬT LÍ
Các aldehyde, ketone có nhiệt độ sôi cao hơn các hydrocarbon có phân tử khối tương đương. Các aldehyde, ketone có mạch carbon ngắn tan tốt trong nước.
Bảng nhiệt độ sôi và độ tan của một số hợp chất carbonyl:
| Công thức | Tên gọi | ts (oC) | Độ tan trong nước ở 20oC (g/100 g) |
|---|---|---|---|---|
Aldehyde | HCHO | methanal | -21 | tan vô hạn |
CH3CHO | ethanal | 20 | tan vô hạn | |
CH3CH2CHO | propanal | 49 | 20 | |
CH3CH2CH2CHO | butanal | 76 | 7 | |
Ketone | CH3COCH3 | propanone | 56 | tan vô hạn |
CH3COCH2CH3 | butanone | 80 | 26 | |
CH3CH2COCH2CH3 | pentan-3-one | 101 | 5 |
Câu hỏi:
@205223832688@
IV. TÍNH CHẤT HÓA HỌC
1. Phản ứng khử
Các hợp chất carbonyl bị khử bởi các tác nhân khử như NaBH4, LiAlH4,... (kí hiệu là [H]).
Aldehyde + 2[H] → Alcohol bậc I
Ketone + 2[H] → Alcohol bậc II
Ví dụ 6:
\(CH_3CH_2CHO+2\left\lbrack H\right\rbrack\rarr CH_3CH_2CH_2OH\)
\(CH_3COCH_2CH_3+2\left\lbrack H\right\rbrack\rarr CH_3CH\left(OH\right)CH_2CH_3\)
2. Phản ứng oxi hóa aldehyde
Aldehyde dễ bị oxi hóa bởi các tác nhân oxi hóa như Br2/H2O, [Ag(NH3)2]OH, Cu(OH)2/OH–,... tạo thành carboxylic acid tương ứng.
a. Oxi hóa aldehyde bởi nước bromine
Aldehyde bị oxi hóa bởi nước bromine tạo thành carboxylic acid.
\(RCHO+Br_2+H_2O\rarr RCOOH+2HBr\)
b. Oxi hóa aldehyde bởi thuốc thử Tollens
- Thuốc thử Tollens oxi hóa aldehyde tạo lớp bạc sáng bám vào thành bình (phản ứng tráng bạc).
\(RCHO+2\left\lbrack Ag\left(NH_3\right)_2\right\rbrack OH\overset{t^{o}}{\rarr}RCOONH_4+2Ag+3NH_3+H_2O\)
- Ketone không bị oxi hóa bởi thuốc thử Tollens.
⚡THÍ NGHIỆM (Aldehyde phản ứng với thuốc thử Tollens)
- Bước 1: Thêm từ từ dung dịch NH3 5% vào 1 mL dung dịch AgNO3 1%. Lắc đến khi kết tủa tan hết.
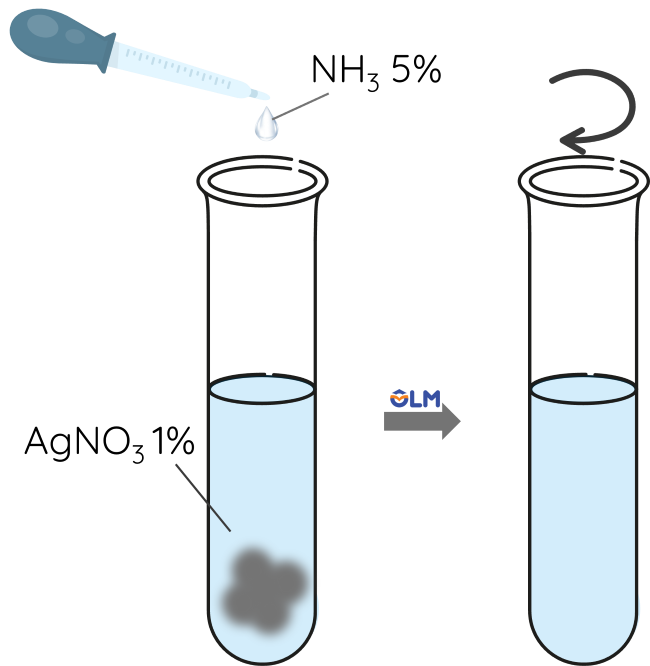
- Bước 2: Nhỏ vài giọt dung dịch CH3CHO 5% vào ống nghiệm, lắc đều.

- Bước 3: Ngâm ống nghiệm vào cốc thủy tinh chứa nước nóng (70 oC - 80 oC) và chờ trong vài phút.
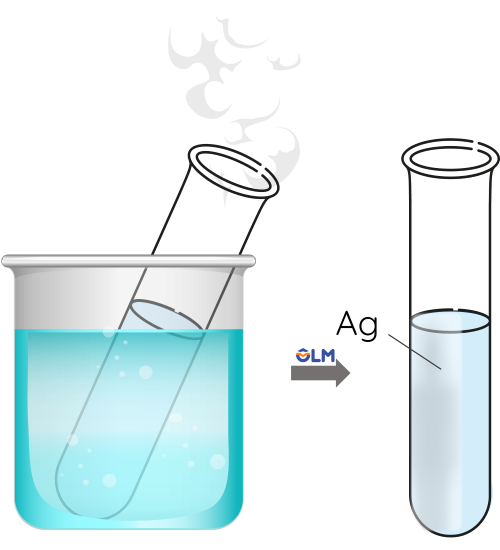
Câu hỏi:
@205223487490@@201219692490@
c. Oxi hóa aldehyde bằng copper(II) hydroxide
Aldehyde bị oxi hóa bởi Cu(OH)2 trong môi trường kiềm khi đun nóng, tạo kết tủa Cu2O màu đỏ gạch.
\(RCHO+2Cu\left(OH\right)_2+NaOH\overset{t^{o}}{\rarr}RCOONa+Cu_2O+3H_2O\)
⚡THÍ NGHIỆM (Phản ứng oxi hóa aldehyde bằng Cu(OH)2)
- Bước 1: Thêm 0,5 mL dung dịch CuSO4 5% vào ống nghiệm chứa 1 mL dung dịch NaOH 10%.
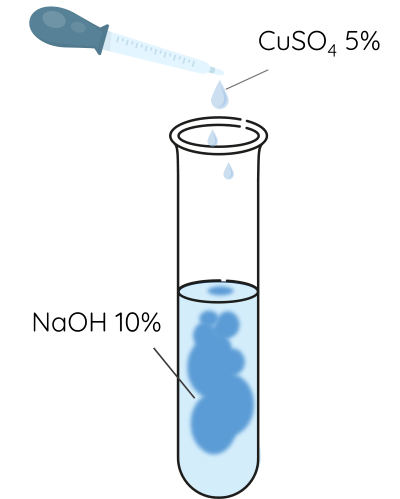
- Bước 2: Thêm tiếp vào ống nghiệm 1 mL dung dịch CH3CHO 5%.

- Bước 3: Đun nóng ống nghiệm bằng ngọn lửa đèn cồn trong vài phút.
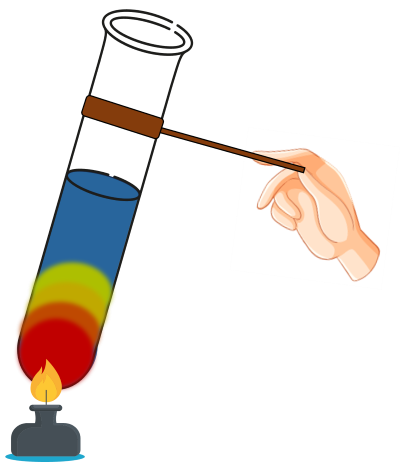
Câu hỏi:
@205223524465@
3. Phản ứng cộng
Hợp chất carbonyl có thể tham gia phản ứng cộng với HCN vào liên kết đôi C = O.

Ví dụ 7:


4. Phản ứng tạo iodoform
Aldehyde và ketone có nhóm methyl cạnh nhóm carbonyl có thể phản ứng với I2 trong môi trường kiềm tạo thành iodoform (CHI3) có màu vàng nhạt, kết tủa.
Ví dụ 8:
\(CH_3COCH_3+3I_2+4NaOH\rarr CH_3COONa+CHI_3+3NaI+3H_2O\)
\(CH_3CHO+3I_2+4NaOH\rarr HCOONa+CHI_3+3NaI+H_2O\)
⚡THÍ NGHIỆM (Phản ứng tạo iodoform từ acetone)
- Bước 1: Thêm 2 mL dung dịch NaOH 2 M và 2 mL dung dịch I2 bão hòa trong KI vào ống nghiệm.

- Bước 2: Cho khoảng 0,5 mL acetone vào ống nghiệm, lắc đều.

Câu hỏi:
@201219696803@
V. ỨNG DỤNG
- Formaldehyde được dùng để sản xuất vật liệu nhựa, keo dán, sơn nổ và bảo quản mẫu sinh vật.
- Acetaldehyde là nguyên liệu để sản xuất acid acetic, acetic anhydride và nhiều hóa chất khác.
- Acetone được sử dụng làm dung môi, cũng như trong sản xuất bisphenol-A và chloroform.

Tiêu bản gan người ngâm trong formol
VI. ĐIỀU CHẾ
Điều chế aldehyde và ketone bằng cách oxi hóa hydrocarbon.
Ví dụ 9: Điều chế acetaldehyde.
\(2CH_2=CH_2+O_2\overset{PdCl_2/CuCl_2}{\rarr}2CH_3CHO\)
Ví dụ 10: Điều chế acetone.

Bạn có thể đăng câu hỏi về bài học này ở đây


